| هیدرولیز یک فرآیند تجزیه شیمیایی است که در آن از آب برای گسستن پیوندهای شیمیایی یک ماده استفاده میشود. این مشخصه واکنش هیدرولیز یا آب کافت با واکنشهایی است که مولکول آب به ترکیب اضافه شده ، اما تکمیلی صورت نمیگیرد. به عبارتی ترکیب شدن یک نمک با آب و تولید اسید و باز را هیدرولیز یا آبکافت گویند و به معنی تجزیه بوسیله آب است. |
نگاه کلی
در
شیمی آلی ترکیباتی وجود دارد که از متراکم شدن دو ترکیب و از دست دادن یک مولکول آب ایجاد میشود. با انجام عمل هیدرولیز روی این ترکیبات میتوان آنها را به ترکیبات سازنده شان تجزیه کرد. عمل هیدرولبز معکوس فرآیند آبگیری یا
تغلیظ میشود و معمولا یک
فرآیند برگشت پذیر میباشد، یعنی با آب گیری از ترکیب هیدرولیز شده دوباره همان ترکیب اولیه حاصل میشود. البته تحت شرایط خاصی هیدرولیز میتواند
برگشت ناپذیر باشد.
چگونگی عمل هیدرولیز
وقتی یک نمک وارد
آب شد، یونیزه میگردد. چون آب ، کمی به صورت
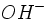
و

یونیزه است، یون مثبت فلزی نمک با یون
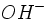
آب به صورت
باز در میآید و یون منفی بنیان نمک با یون

آب تولید
اسید میکند. این عمل آب را
هیدرولیز گویند.
مثلا وقتی NaCl وارد آب میشود، به یونهای
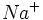
و
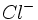
تفکیک میگردد. یون
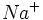
نمک با یون
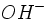
آب تولید NaOH و یون
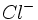
نمک با یون

آب تولید HCl مینماید، ولی چون هم NaOH و هم HCl از دسته بازها و اسیدهای قوی هستند و بلافاصله بطور صددرصد یونیزه میشوند و یونهای
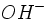
و

آب را مجددا آزاد میسازند، تاثیری بر تعادل یونی
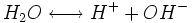
که همیشه در
آب مقطر برقرار است، نمیگذارند و با توجه به اینکه در آب مقطر

و
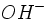
با هم برابرند، با حل شدن NaCl در آب به هیچ تغییری در PH آب پدید نمیآید.
بنابراین محلول خنثی است و هیچ اثری بر
معرفهای شیمیایی ندارد. به همین دلیل میگویند یونهای
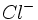
و
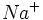
در آب هیدرولیز نمیشوند. بنابراین میتوان گفت که یونهای مولد اسید و باز قوی ، در آب هیدرولیز نمیشود.
انواع هیدرولیز
هیدرولیز استرها
یک
استر ترکیب متراکم شده از
الکل و
اسید کربوکسیلیک میباشد. از فرآیند هیدرولیز ، استر در حضور آب و اسید قوی حرارت داده شده و با شکستن مولکول استر دو فرآورده ایجاد میشود که یکی شامل
گروه هیدروکسیل (OH) و فرآوردههای دیگر شامل گروه عاملی اسید کربوکسیلیک میباشد. قسمتی از مولکول مادر که از ابتدا به صورت کربوکسیلات بوده
هیدروژن آب اضافه شده را دریافت میکند و قسمتی که شامل
گروه آلکیل بوده ، گروه هیدروکسیل باقیمانده از مولکول آب را دریافت کرده و به الکل تبدیل میشود.
با فرآیند آبگیری
'RCOOH + OH-R' → R-COOR
فرآیند هیدرولیز
R-COO-R → R-COOH + ROH
هیدرولیز استر میتواند در محیط اسیدی یا بازی انجام گیرد. بر خلاف هیدرولیز با کاتالیست اسیدی که برگشت پذیر است، هیدرولیز از طریق کاتالیست بازی برگشت ناپذیر است، زیرا واکنش در مرحله آخر به طرف کامل شدن پیش رفته و اسید کربوکسیلیک به یون
کربوکسیلات تبدیل میشود.
هیدرولیز آمینو اسیدها
آمینو اسیدها ترکیبات دوگانهای از
اسید کربوکسیلیک و
آمین هستند. در هیدرولیز این ترکیبات قسمتی از مولکول مادر که قسمت اسید کربوکسیلیک میباشد، گروه
-OH آب را جذب کرده و قسمت آمین
+H را جذب میکند.
هر نمکی که محلول آن در آب از نظر خاصیت اسیدی و بازی خنثی باشد، آن را
نمک خنثی مینامند. هر نمکی که از ترکیب اسیدی قوی با باز قوی بوجود آمده باشد و بر اثر هیدرولیز در آب همین اسید و باز را با ظرفیت برابر تولید نماید، محلولش در آب ، خنثی است.
- مثال1 : معادله هیدرولیز NaCl در آب را به شکل زیر مینویسیم:
محلول خنثی است.
- مثال 2 :معادله هیدرولیز سولفات سدیم (
 ) را به شکل زیر مینویسیم:
) را به شکل زیر مینویسیم:
محلول خنثی است.
نمکی از اسید و باز ضعیف عمل هیدرولیز
اگر نمکی از ترکیب یک باز ضعیف با یک اسید ضعیف بوجود آمده باشد، وقتی در آب حل و یونیزه میگردد، همه یونهای حاصل از آن در آب هیدرولیز میشوند. زیرا وقتی یونهای

و
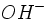
آب را میگیرند، به صورت اسید و باز ضعیف در میآیند و قسمت عمده مولکولهای آنها یونیزه نمیشوند و اگر ظرفیتها و
درجه تفکیک یونی اسید و باز حاصل با هم برابر باشند، محلول خنثی خواهد بود. مانند
استات آمونیوم در آب:
که
 هیدروکسید آمونیوم
هیدروکسید آمونیوم (باز ضعیف) با
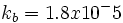
و
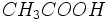 اسید استیک
اسید استیک (اسید ضعیف) با

میباشد. محلول خنثی است، چون محصولات هم ظرفیتهای برابر دارند و هم ثابت تفکیک یونی برابر.
نمکی از اسید قوی و عمل هیدرولیز
اگر نمکی از ترکیب یک اسید قوی با یک باز ضعیف بوجود آمده باشد، مثل
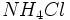
(از ترکیب
اسید کلریدریک با هیدروکسید آمونیوم) و در آب حل و یونیزه گردد، یون بنیان آن هیدرولیز نمیشود، چون مربوط به اسید قوی است و اگر هم با یون

آب ترکیب شود، بلافاصله تفکیک میگردد و تاثیری بر تعادل یونی آب نمیگذارد. ولی یون مثبت آن با یون
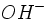
آب به صورت یک باز ضعیف در میآید و باعث کاهش تعداد یونهای
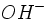
میگردد و محیط را اسیدی میکند. اینگونه نمکها را
نمک اسیدی گویند.
محلول اسیدی است.
نمکی از باز قوی و عمل هیدرولیز
اگر نمکی از ترکیب یک باز قوی با یک اسید ضعیف بوجود آمده باشد و در آب حل و یونیزه شود، یون فلزی آن که متعلق به باز قوی است، هیدرولیز نمیشود و تاثیری بر تعادل یونی آب نمیگذارد، زیرا اگر هم با یون
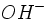
آب به صورت باز در آید، بلافاصله تفکیک میگردد، ولی بنیانهای اسیدی این نمک با گرفتن یونهای

آب به صورت مولکولهای اسید ضعیف در میآیند و قسمت عمده یونهای

گرفته را آزاد نمیسازند و باعث کاهش یون

در آب و جابجایی تعادل یونی آب در جهت تولید یون

و در نتیجه افزایش یون
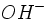
شده و محیط را قلیایی میسازند. مثل
کربنات سدیم:
محیط قلیایی است.
هیدرولیز نمکی از اسید و باز قوی با ظرفیتهای متفاوت
اگر از هیدرولیز یک نمک در آب اسید و باز قوی تولید شوند، ولی ظرفیتهای آنها برابر نباشند و یا درجه تفکیک یونی آنها برابر نباشند، محلول حاصل ، خاصیت جسم قویتر و یا خاصیت جسم دارای ظرفیت بیشتر را خواهد داشت. مثلا اگر یک مول
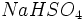
وارد مقداری آب شود، تولید یک مول NaOH و یک مول
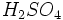
در آب میکند. 2 مول یون

آزاد میشوند. یک مول
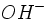
با یک مول

اسید خنثی میشود و یک مول دیگر از یونهای

اسید بطور اضافی در محیط باقی میماند و محیط را اسیدی میکند:
برگشت ناپذیری هیدرولیز در شرایط فیزیولوژیکی
همانگونه که اشاره شد هیدرولیز را میتوان وارونه
واکنش تراکم در نظر گرفت در بین دو ترکیبی که با اتصال به هم یک
مولکول آب از دست میدهند. بنابراین آب گیری و هیدرولیز میتوانند در برخی موقعیتها در حال تعادل باشند. اما تحت شرایط فیزیولوژیکی ، جایی که غلظت یک پیش ماده متابولیک پایین است، واکنش هیدرولیز بطور ترمودینامیکی برگشت ناپذیر میباشد.
برای مثال
A + H2O → X + Y
با فرض اینکه X غلظت نهایی و Y غلظت اولیه A باشد، اگر Y/X کمتر از 0.01 درصد غلظت واکنش دهنده اولیه باشد، هیدرولیز برگشت ناپذیر خواهد بود.
مباحث مرتبط با عنوان