اطلاعات اولیه
|
|
| نام آیوپاک | نامهای دیگر | فرمول شیمیایی | وزن مولکولی | نقطه جوش | نقطه ذوب | PH
|
| اتانول | اتیل الکل ، الکل اتیلیک |  | 46.069gr/mol | 78.4 درجه سانتیگراد | 114.3- درجه سانتیگراد | 7 |
|
|
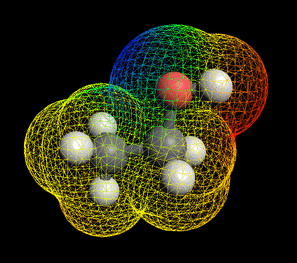
ساختمان اتانول
|
تاریخچه
اتانول برای انسان از دوران باستان شناخته شده بود، زیرا این ماده ، جزء اصلی مشروبات الکلی است. جداسازی آن بصورت اتانول نسبتا خالص احتمالا اولین بار توسط "
جابر بن حیان" که صنعت
تقطیر را گسترش داد، انجام شده است. البته بیشتر گمان میرود که اتانول خالص توسط "
محمد زکریای رازی" دانشمند ایرانی تولید شده باشد.
فرایند تولید
اتانول مورد استفاده در نوشابههای الکلی توسط فرایند تخمیر از متابولیسم
گلوکز توسط گونه مخصوصی از مخمرها در غیاب
اکسیژن تولید میشود و در پایان فرایند تخمیر غلظت اتانول را با
تقطیر بالا میبرند. برای مخلوط اتانول با
آب بالاترین نقطه آزئوتروپ جوش برای 95%
الکل و 5%
آب است. بنابراین جزء تقطیر شده مخلوط اتانول و آب نمیتواند خالصتر از 95 درصد باشد. برای تولید اتانول خالصتر ، مقدار کمی
بنزن به آن اضافه میشود.
بنزن ، آزئوتروپ سهگانه ای با آب و اتانول تشکیل میدهد و مخلوط دوباره تقطیر میشود. نتیجه این فرایند بدست آوردن اتانول بدون آب است. با این همه چند ppm بنزن در اتانول باقی میماند که جذب آن در بدن از مشخصههای آسیب کبدی است که در افراد الکلی دیده میشود.
تولید اتانول صنعتی
اتانول سوخت نسبتا خوبی برای موتورهاست و در صنعت ، بصورتهای مختلفی استفاده میشود. اتانول مورد مصرف در صنعت را معمولا از واکنش
کاتالیزوری آب با
اتیلن تولید میکنند. این یک واکنش افزایشی است که در آن یک
مولکول آب شکافته شده ، قطعات حاصل از آن به اتمهای
کربن در پیوند دوگانه اضافه میشود. این فرایند ، تولید اتانول اقتصادیتر از تولید آن با مخمر است.
امروزه برای تولید تجارتی آسان آن تخمیر مواد آلی زائد مانند خرده چوب و خاک اره پیشنهاد شده است. اتانول صنعتی برای مصرف انسان ، نامناسب است، زیرا به آن ، مقادیر کمی
متانول و مواد سمی دیگر اضافه میشود.
خواص فیزیکی
اتانول ، مایعی قابل احتراق و بیرنگ بوده ، یکی از انواع الکلهای موجود در نوشابههای الکلی است.
گرانروی آن ، مانند آب است و بوی نسبتا تندی دارد. در صنعت بعنوان حلال و ماده واسطه شیمیایی برای تولید بیشتر ترکیبات آلی استفاده میشود. بدلیل تشکیل
پیوند هیدروژنی با هر نسبتی در آب حل میشود. اتانول در مقایسه با ترکیبات آلی که وزن مولکولی یکسانی با آن دارند،
نقطه جوش بالاتری دارد.
به عنوان مثال نقطه جوش پروپان که تقریبا وزن مولکولی برابری با اتانول دارد، 43- درجه سانتیگراد است، درحالیکه نقطه جوش اتانول 78 درجه سانتیگراد است. دلیل این اختلاف ، وجود پیوندهای هیدروژنی مربوط به گروه
OH است که نیروی جاذبه میان مولکولهای مجاور را افزایش میدهد. اتانول خاصیت ضعیف اسیدی و بازی از خود نشان میدهد که خاصیت بازی آن بدلیل
جفت الکترون تنهای اکسیژن بوده و خاصیت اسیدی آن ، بخاطر پیوند
هیدروژن با
عنصر الکترونگاتیو
اکسیژن است. اتانول با فلزات فعال ( Na و K و Mg و … ) وارد واکنش شده ،
اتوکسید ایجاد میکند.
کاربرد
اتانول بدلیل نقطه ذوب پائین در صنعت ضدیخسازی استفاده میشود. حلال بسیار خوبی است و در صنعت عطرسازی ، رنگسازی و … استفاده میشود. محلول %85 – 70 آن بعنوان محلول ضدعفونی کننده کاربرد دارد. اتانول با تغییر دادن
پروتئین و حل کردن
چربی ، میکرو ارگانیسمهای آنها را از بین میبرد. البته این عمل فقط در برابر
باکتریها و
ویروسها و
قارچها موثر است، ولی در مقابل هاگ ، باکتریها تاثیری ندارد. اتانول همچنین در صنایع مشروبات الکلی به میزان گسترده ای مورد استفاده قرار میگیرد.
|
|
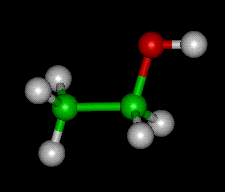
ساختمان اتانول
|
نکته مهم
مصرف بیش از حد مشروبات الکلی ، بدلیل وجود اتانول در ترکیب آنها باعث ایجاد عوارض بسیاری در سلامتی انسان میشود که عبارتند از :
عوارض حاد
تهوع ، استفراغ ، افسردگی ، تنگی نفس.
عوارض مزمن
اعتیاد به الکل (الکسیم) ، سایروز کبدی ، تاثیر در سلسله
اعصاب مرکزی ، تاثیر در
حافظه در بلند مدت.
مباحث مرتبط با عنوان